A coninuacion les presento un video sobre el atomo para comenzar con la cronologia del desarrolo de los modelos atomicos
Ya vimos lo que es un atomo, ahora comenzemos con la cronologia de los modelos atomicos, primero vamos con Democrito sobre su postulado del atomo.
Democrito
Demócrito de Abdera vivió entre los años 460 al 370 aC, siendo contemporáneo a Sócrates. Hiparco de Nicea asegura, según Diógenes de Laertes, que Demócrito murió a los 90 años de edad; y todos los autores de la antigüedad que hayan hecho referencia a su edad, coinciden en que vivió más de cien años. Fue conocido en su época por su carácter extravagante, ya que según relatos solía reír muy a menudo. Se dice que viajó por Egipto, Caldea y Persia y que incluso llegó a la India en busca de conocimientos. Una leyenda dice que se arrancó los ojos en un jardín para que no le estorbara en la contemplación del mundo externo en sus meditaciones; leyenda que expresa el desprecio que Demócrito tenía por el conocimiento meramente sensitivo.
Diógenes de Laertes listó una serie de escritos de Demócrito que superan las 70 obras sobre ética, física, matemática, técnica e incluso música, por lo que Demócrito es considerado un autor enciclopédico. Demócrito es considerado fundador de la escuela atomista.
Para Demócrito, la realidad está compuesta por dos causas (o elementos), lo que es, representado por los átomos homogéneos e indivisibles, y lo que no es, representado por el vacío. Este último es un no-ser no-absoluto, aquello que no es átomo, el elemento que permite la pluralidad de partículas diferenciadas y el espacio en el cual se mueven.
Demócrito pensaba y postulaba que los átomos son indivisibles, y se distinguen por forma, tamaño, orden y posición.
Para Demócrito, los átomos estuvieron y estarán siempre en movimiento y son eternos. El movimiento de los átomos en el vacío es un rasgo inherente a ellos, un hecho irreductible a su existencia, infinito, eterno e indestructible.
Al formar los átomos, por necesidad, un vórtice o remolino (dine), sus colisiones, uniones y separaciones forman los diferentes objetos y seres y la realidad con toda su diversidad. Cada objeto que surge en el universo y cada suceso que se produce, sería el resultado de colisiones o reacciones entre átomos. Aunque la cita "todo cuanto existe es fruto del azar y la necesidad" se atribuye a Demócrito, sus escritos enfatizan en la necesidad. El modelo atomista constituye un claro ejemplo de modelo materialista, dado que el azar y las reacciones en cadena son las únicas formas de interpretarlo.
La psyché (alma) del hombre estaría formada por átomos esféricos livianos, suaves, refinados y el soma (cuerpo), por átomos más pesados. Las percepciones sensibles, tales como la audición o la visión, son explicables por la interacción entre los átomos de los efluvios que parten de la cosa percibida y los átomos del receptor. Esto último justifica la relatividad de las sensaciones.
El conocimiento verdadero y profundo es el de los átomos y el vacío, pues son ellos los que generan las apariencias, lo que percibimos, lo superficial.

Aqui les dejo un video sobre Democrito:
Modelo atómico de John Dalton
La observación de las cantidades fijas en las que diferentes sustancias químicas se combinaban para reaccionar químicamente, llevó a Dalton a la hipótesis de que existía una cantidad mínima o discreta de materia de cada sustancia que se combinaba de manera fija con un cierto número de unidades fijas de otras sustancias. Dalton observó que muchas sustancias podían considerarse como compuestas por diferentes especies de materia, y consecuentemente clasificó a todas las sustancias en:
- Elementos, o sustancias químicas simples formadas por una única especie de materia.
- Sustancias compuestas, que podían considerarse como formadas por proporciones fijas de diferentes elementos.
De acuerdo con esa idea Dalton llamó átomo a la cantidad mínima de un elemento dado. Y más tarde se llamaría molécula a una combinación de un número entero de átomos que parecía ser la cantidad mínima de cada sustancia que podía existir. El modelo atómico de Dalton asumía que los átomos eran de hecho indivisibles y sin estructura interna, de hecho, por eso escogió denominarlos a partir de la palabra griega átomos 'sin partes, sin división'.
- El modelo atómico de Dalton explicaba porqué las sustancias se combinaban químicamente entre sí sólo en ciertas proporciones.
- Además el modelo aclaraba que aún existiendo una gran variedad de sustancias diferentes, estas podían ser explicadas en términos de una cantidad más bien pequeña de constituyentes elementales o elementos.
- En esencia, el modelo explicaba la mayor parte de la química orgánica del siglo XIX, reduciendo una serie de hechos complejos a una teoría combinatoria realmente simple.
Dalton explicó su teoría formulando una serie de enunciados simples:.
- La materia está formada por partículas muy pequeñas llamadas átomos, que son indivisibles y no se pueden destruir.
- Los átomos de un mismo elemento son iguales entre sí, tienen su propio peso y cualidades propias. Los átomos de los diferentes elementos tienen pesos diferentes.
- Los átomos permanecen sin división, aún cuando se combinen en las reacciones químicas.
- Los átomos, al combinarse para formar compuestos guardan relaciones simples.
- Los átomos de elementos diferentes se pueden combinar en proporciones distintas y formar más de un compuesto.
- Los compuestos químicos se forman al unirse átomos de dos o más elementos distintos.
Sin embargo desapareció ante el modelo de Thomson ya que no explica los rayos catódicos, la radioactividad ni la presencia de los electrones (e-) o protones(p+).
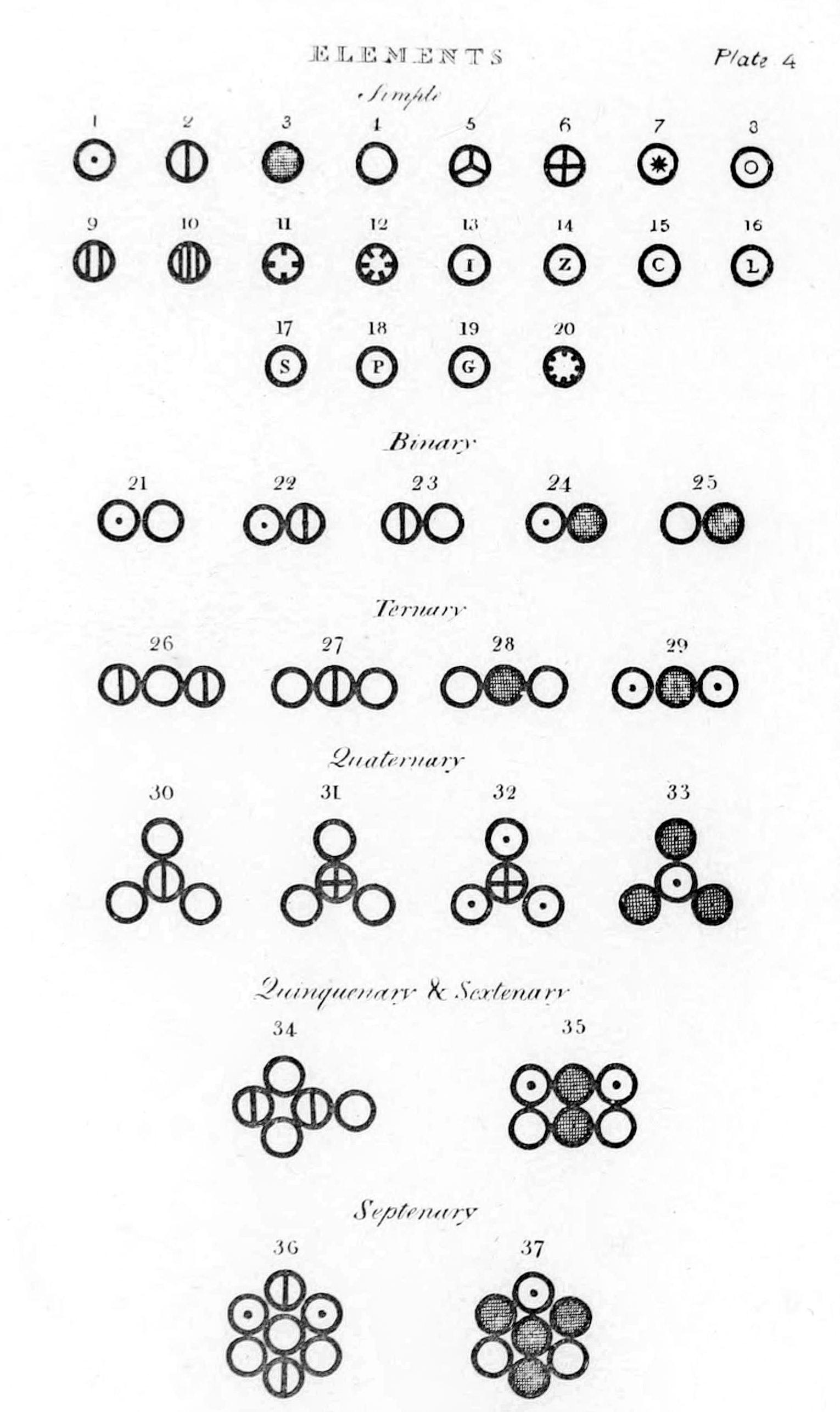
Varios átomos y moléculas representados en A New System of Chemical Philosophy (1808) de John Dalton.

Esta es una representacion de lo que era el atomo para Dalton, una esfera.
Les dejo un video en cual se muestra una animacion en la que Dalton nos dice como se formaban los compuestos quimicos en su modelo. Ademas podemos apreciar que el creia que los atomos se enganchaban para fromar los compuestos quimicos
Modelo atómico de Thomson
El "modelo atómico de Thomson", también conocido como el pastel de pasas, es una teoría sobre la estructura atómica propuesta en 1904 por Joseph John Thomson, descubridor del electrón, antes del descubrimiento del protón y del neutrón. En dicho modelo, el átomo está compuesto por electrones de carga negativa en un átomo positivo, como pasas en un budín. Se pensaba que los electrones se distribuían uniformemente alrededor del átomo. En otras ocasiones, en lugar de una sopa de carga positiva se postulaba con una nube de carga positiva. En 1906 Thomson recibió el premio Nobel de la Paz por este descubrimiento.
Dado que el átomo no deja de ser un sistema material que contiene una cierta cantidad de energía externa, ésta provoca un cierto grado de atracción de los electrones contenidos en la estructura atómica. Desde este punto de vista, puede interpretarse que el modelo atómico de Thomson es un modelo actual como consecuencia de la elasticidad de los electrones en el coseno de la citada estructura.
Si hacemos una interpretación del modelo atómico desde un punto de vista más microscópico, puede definirse una estructura abierta para el mismo dado que los protones se encuentran inmersos y sumergidos en el seno de la masa que define la carga neutra del átomo.
Dicho modelo fue superado luego del experimento de Rutherford, cuando se descubrió el núcleo del átomo. El modelo siguiente fue el modelo atómico de Rutherford.
Cabe mencionar que para llegar al modelo atomico de Thomson, se desarrollaron experimentos como: el descubrimiento de los rayos catodicos por Julius Plücker y Heinrich Geissler, tambien con un experimento similar tenemos a William Crookes, el experimento de la gota de aceite de Robert Andrews Millikan, el experimento de E. Goldstein con el tuvo de rayos canales y el tubo de rayos catodicos de Thomson.
A continuacion veremos los diferentes experimentos que realizaron estos personajes para comprobar la presencia de algunas particulas subatomicas.
Julius Plücker

Plücker nació en Elberfeld (ahora parte de Wuppertal). Después de ser educado en Düsseldorf y las universidades de Bonn, Heidelberg y Berlín fue a París en 1823, donde encontró la influencia de la gran escuela de geómetras, cuyo fundador, Gaspard Monge, había muerto recientemente. En 1825 volvió a Bonn, y en 1828 se hizo catedrático en matemática. En el mismo año publicó el primer volumen de su Analytisch-geometrische Entwickelungen, que introdujo por primera vez el método de anotación abreviada. En 1831 publicó el segundo volumen, en el cual estableció la dualidad proyectiva en una base sólida e independiente.
En 1847 Plücker comenzó a dar clases como profesor de física en Bonn. En 1858 publicó la primera de sus investigaciones clásicas sobre la acción del imán sobre la descarga eléctrica en los gases enrarecidos. Descubrió que la descarga hizo que un brillo fluorescente formara en las paredes vidrios del tubo de vacío, y que se pudo mover el brillo si se aplica un electroimán al tubo, así creando un campo magnético. Después se mostró que el brillo fue producido por rayos catódicos.
Plücker, principalmente solo y después junto con Johann Hittorf, hizo muchos descubrimientos importantes en la espectroscopia de gases. Fue el primer emplear el tubo de vacío con la parte capilar (ahora llamado un tubo de Geissler), a través del cual podía aumentar la intensidad luminosa de las descargas eléctricas a un nivel suficiente para dejar la investigación espectroscópica. Previó Robert Wilhelm Bunsen y Gustav Kirchhoff en anunciar que las líneas del espectro fueron características de la sustancia química que las emitió, y en la indicación del valor de este descubrimientos en el análisis químico. Según Hittorf fue el primer quien vio las tres líneas del espectro de hidrógeno, que pocos meses después de su muerte fueron reconocidas en el espectro de las protuberancias solares.
En 1865 Plücker volvió al campo de geometría e inventó lo que se llamaba la geometría de líneas durante el siglo XIX. En la geometría proyectiva, las coordenadas Plücker refieren a una colección de coordenadas homogéneas introducidas inicialmente para enterrar la colección de líneas en tres dimensiones como una cuádrica en cinco dimensiones. La construcción usa determinantes menores 2×2, o igualmente el segundo producto exterior del espacio vectorial subyacente del cuarto dimensión. Ahora forma parte de la teoría de Grassmannian, en la cual estas coordenadas aplican en la generalidad (subespacios en la dimensión k del espacio de la dimensión n).
Plücker fue galardonado con la Medalla Copley de la Sociedad Real en 1866.
Heinrich Geissler

Geissler dominaba la técnica del soplado de cristal y poseía un negocio de fabricación de instrumentos científicos. En 1857 inventó una bomba de vacío sin elementos mecánicos móviles, basada en los trabajos de Evangelista Torricelli. Aprovechando el vacío creado por el descenso de la columna de mercurio encerrada en el interior de un tubo, consiguió alcanzar niveles de vacío no conseguidos con anterioridad. Los recipientes en los que se practica el vacío de esta manera, llamados "Tubos de Geissler", tuvieron un papel muy importante en los experimentos de descarga en tubos de vacío y contribuyeron al estudio de la electricidad y de los átomos.
Aqui le presento unos videos para que se den una idea de que es un tubo de geiser
William Crookes

Sir William Crookes (17 de junio de 1832- 4 de abril de 1919) fue un químico inglés, uno de los científicos más importantes en la Europa del Siglo XIX, tanto en el campo de la física como en el de la química. Estudió en el Colegio Real de Química de Londres. Fundó la revista de divulgación Chemical News, y fue editor del Quarterly Journal for Science. En 1863 entró a la Royal Society recibiendo la prestigiosa medalla para 1875. En 1888 recibe la Medalla Davy, fue nombrado caballero en 1897, la Medalla Copley en 1904 y en 1910 fue nombrado “Sir” recibiendo la Orden del Mérito.
Investigación científica
Crookes descubrió el elemento metálico talio y desarrolló un proceso de amalgación para separar la plata y el oro de sus minerales. En química aplicada trató diversos temas: tratamiento de las aguas de las cloacas, la fabricación del azúcar de remolacha, el tinte de tejidos, entre otros. Sin embargo, su trabajo más importante fue la investigación sobre la conducción de la electricidad en los gases. Inventó el tubo de Crookes, para el estudio de las propiedades de los rayos catódicos; y también inventó el radiómetro, y el espintariscopio, un detector de partícula. Entre sus trabajos más importantes está el haber sido el primero en identificar el Plasma (estado de la materia)
Sobre el Radiómetro de Crookes (también llamado molinito de luz o light-mill en inglés): Crookes utilizó en éste una bomba de Sprengel. Esta bomba consiste en un tubo capilar de vidrio de una altura aproximadamente de 76 cm. En su parte superior lleva una especie de embudo que contiene mercurio (aproximadamente 12 kg) y en la parte de abajo un recipiente para recibir las gotas. Si se terminaba el mercurio de arriba era cuestión de vaciar el que había bajado. Las gotas de mercurio al bajar por efecto de la gravedad lentamente extraen pequeñas porciones de aire del bulbo al que se quiere hacer vacío. Para llegar a la presión del radiómetro de necesitaron de 6 a 8 horas. Es por eso que Crookes pudo observar lentamente el inicio del giro del radiómetro sin necesidad de medir la presión. Con algunos arreglos en la bomba de Sprengel, Crookes pudo llegar a tal presión.
Este es un tubo de Crookes
Video de el del exmerimento del radiometro de Crookes
Robert Andrews Millikan

Robert Andrews Millikan en 1891.Robert Andrews Millikan (n. Morrison, Illinois; 22 de marzo de 1868 - † San Marino, California; 19 de diciembre de 1953) fue un físico estadounidense que ganó el Premio Nobel de Física en 1923 primordialmente por su trabajo para determinar el valor de la carga del electrón y el efecto fotoeléctrico. También investigó los rayos cósmicos.
Estudió en un principio la radioactividad de los minerales de uranio y la descarga en los gases. Luego realizó investigaciones sobre radiaciones ultravioletas.
Este es un video en donde se muestra una animacion del experimento de Millikan, esta en ingles
pero emsegida les explicare en que consiste
Experimento de Millikan
Se denomina experimento de Millikan o experimento de la gota de aceite al experimento realizado por primera vez en 1909 por el físico estadounidense Robert Millikan y que le permitió medir la carga del electrón.
El experimento consiste en introducir en un elemento gaseoso, gotitas de aceite de un radio del orden de un micrómetro. Estas gotitas caen lentamente, con un movimiento uniforme, con su peso compensado por la viscosidad del medio. Este tipo de movimiento viene regido por la ley de Stokes. Ahora bien, las gotas se cargan electrostáticamente al salir del atomizador por lo que su movimiento de caída se altera significativamente si se hace actuar un campo eléctrico vertical. Ajustando convenientemente la magnitud del campo eléctrico, puede lograrse que la gota permanezca en suspensión.
Conociendo el valor m de la masa de la gota, la intensidad E del campo eléctrico y el valor g de la gravedad, puede calcularse la carga q de la gota en equilibrio:
mg = qE principalmente
Millikan comprobó que los valores de las cargas eran siempre múltiplos de una carga elemental, la del electrón. Por consiguiente pudo medir la carga eléctrica que posee un electrón. Este valor es:
e = 1,602 × 10-19 culombios.
Millikan recibió el premio Nobel de Física en 1923 en parte por este experimento.
Eugen Goldstein

Eugene Goldstein (5 de septiembre, 1850 – 25 de diciembre, 1930) fue un físico alemán. Fue un temprano investigador de Rayos X.
Fue profesor de la Universidad de Berlín. Se dedicó a investigar las descargas en los gases enrarecidos. Oponiéndose a Crookes, creyó que los rayos catódicos eran, a semejanza de la luz, de naturaleza ondulatoria.
En 1886 observó por primera vez a los protones desde los rayos catodicos.
Los planteamientos de Goldstein fueron los que le dieron la posibilidad a Thomson para que los recogiera y formulara el modelo atómico de Thomson.
Fue enterrado en el Weißensee Cemetery.
También trabajó como abogado de Inmigración Judía.
Goldstein nació en 1850 en Gleiwitz la Alta Silesia, ahora conocido como Gliwice, Polonia. Estudió en Breslau, y más tarde, en virtud de Helmholtz, en Berlín. Goldstein, trabajó en el Observatorio de Berlín desde 1878 hasta 1890, pero pasó la mayor parte de su carrera en el Observatorio de Potsdam, donde se convirtió en jefe de la sección de astrofísica en 1927. Murió en 1930 y fue enterrado en el cementerio de Weissensee en Berlín.
A mediados del siglo XIX, Julius Plücker investigó la luz emitida en los tubos de descarga y la influencia de campos magnéticos en el resplandor. Más tarde, en 1869Johann Wilhelm Hittorf estudiado tubos de descarga de rayos de energía que se extiende desde un electrodo negativo, el cátodo. Estos rayos de fluorescencia producida cuando golpean las paredes de vidrio de un tubo, y cuando es interrumpido por un objeto sólido que arrojan una sombra.
En la década de 1870 Goldstein había realizado sus propias investigaciones de los tubos de descarga, y nombró a las emisiones de luz estudiados por otros kathodenstrahlen, o los rayos catódicos. En 1886, descubrió que los tubos de descarga de cátodo perforado también emiten una luz al final del cátodo. Goldstein llegó a la conclusión que, además de los rayos catódicos ya conocida, posteriormente reconocido como electrones que se mueven desde el cátodo con carga negativa hacia el ánodo cargado positivamente, no hay otro rayo que viaja en la dirección opuesta. Debido a que estos últimos rayos pasa a través de los agujeros, o canales, en el cátodo, Goldstein llamó kanalstrahlen, o los rayos del canal. Están compuestos de iones positivos, cuya identidad depende de la de gas residual en el interior del tubo. Fue otro de los estudiantes de Helmholtz, Wilhelm Wien, que más tarde llevó a cabo extensos estudios de los rayos del canal, y en el tiempo esta obra se convertiría en parte de la base de la espectrometría de masas.
El rayo de ánodo con la menor relación E / m proviene del gas hidrógeno (H2), y está hecho de iones H +. En otras palabras, este rayo es de protones. Trabajo de Goldstein con los rayos de ánodo de H + fue aparentemente la primera observación de que el protón, aunque estrictamente hablando se podría argumentar que era Wien, que mide la relación E / m del protón y tiene el mérito de su descubrimiento.
Goldstein también se utilizan tubos de descarga para investigar cometas. Un objeto, como una pequeña bola de cristal o de hierro, colocados en el camino de los rayos catódicos produce emisiones secundarias a los lados, hacia el exterior en la quema de una manera que recuerda la cola de un cometa.
tubo de rayos catodicos
}
Esto es lo que hizo thomson para comprobar la carga que tenia los rayos catodicos
Aqui les dejo un video con el modelo atomico de Thomson y los rayos catodicos
Ahora pasemos con el modelo atomico de Rutherford
Modelo atómico de Rutherford

El modelo atómico de Rutherford es un modelo atómico o teoría sobre la estructura interna del átomo propuesto por el químico y físico británico Ernest Rutherford para explicar los resultados de su "experimento de la lámina de oro", realizado en 1911.
La importancia del modelo de Rutherford residió en proponer la existencia de un núcleo en el átomo. Término que, paradójicamente, no aparece en sus escritos. Lo que Rutherford consideró esencial, para explicar los resultados experimentales, fue "una concentración de carga" en el centro del átomo, ya que si no, no podía explicarse que algunas partículas fueran rebotadas en dirección casi opuesta a la incidente. Este fue un paso crucial en la comprensión de la materia, ya implicaba la existencia de un núcleo atómico donde se concentraba toda la carga positiva y más del 99,9% de la masa. Las estimaciones del núcleo revelaban que el átomo en su mayor parte estaba vacío.
Rutherford propuso que los electrones orbitarían en ese espacio vacío alrededor de un minúsculo núcleo atómico, situado en el centro del átomo. Además se abría varios problemas nuevos que llevarían al descubrimiento de nuevos hechos y teorías al tratar de explicarlo:
Por un lado se planteó el problema de como un conjunto de cargas positivas podían mantenerse unidas en un volumen tan pequeño, hecho que llevó posteriormente a la postulación y descubrimiento de la fuerza nuclear fuerte, que es una de las cuatro interacciones fundamentales.
Por otro lado existía otra dificultad proveniente de la electrodinámica clásica que predice que una partícula cargada y acelerada, como sería necesario para mantenerse en órbita, radiaría radiación electromagnética, perdiendo energía. Las leyes de Newton, junto con las ecuaciones de Maxwell del electromagnetismo aplicadas al átomo de Rutherford llevan a que en un tiempo del orden de 10 − 10s, toda la energía del átomo se habría radiado, con la consiguiente caida de los electrones sobre el núcleo. Se trata, por tanto de un modelo físicamente inestable, desde el punto de vista de la física clásica.
Aunque según Rutherford, las órbitas de los electrones no están muy bien definidas y forman una estructura compleja alrededor del núcleo, dándole un tamaño y forma algo indefinidas. No obstante, los resultados de su experimento, permitieron calcular que el radio del átomo era diez mil veces mayor que el núcleo mismo, lo que hace que haya un gran espacio vacío en el interior de los átomos.
El modelo atómico de Rutherford fue sustituido muy pronto por el de Bohr. Bohr intentó explicar fenomenológicamente que sólo algunas órbitas de los electrones fueran posibles. Lo cual daría cuenta de los espectros de emisión y absorción de los átomos en forma de bandas discretas
El modelo de Bohr "resolvía" el problema proveniente de la electrodinámica postulando que sencillamente los electrones no radiaban, hecho que fue explicado por la mecánica cuántica según la cual la aceleración promedio del electrón deslocalizado era nula.
modelo atomico de Rutherford

Les dejo con unos videos del experimento que realizo rutherford con la lamina de oro
Experiemto de la lamina de oro
Experimento de Rutherford
El experimento de Rutherford, también llamado "experimento de la lámina de oro", fue realizado por Hans Geiger y Ernest Marsden en 1909, bajo la dirección de Ernest Rutherford en los Laboratorios de Física de la Universidad de Manchester. Los resultados obtenidos y el posterior análisis tuvieron como consecuencia la rectificación del modelo atómico de Thomson (modelo atómico del panqué con pasas) y la propuesta de un modelo nuclear para el átomo.
El experimento consistió en "bombardear" con un haz de partículas alfa una fina lámina de oro y observar cómo las láminas de diferentes metales afectaban a la trayectoria de dichos rayos.
Las partículas alfa se obtenían de la desintegración de una sustancia radiactiva, el polonio. Para obtener un fino haz se colocó el polonio en una caja de plomo, el plomo detiene todas las partículas, menos las que salen por un pequeño orificio practicado en la caja. Perpendicular a la trayectoria del haz se interponía la lámina de metal. Y, para la detección de trayectoria de las partículas, se empleó una pantalla con sulfuro de zinc que produce pequeños destellos cada vez que una partícula alfa choca con él.
Según el modelo de Thomson, las partículas alfa atravesarían la lámina metálica sin desviarse demasiado de su trayectoria:
La carga positiva y los electrones del átomo se encontraban dispersos de forma homogénea en todo el volumen del átomo. Como las partículas alfa poseen una gran masa (8.000 veces mayor que la del electrón) y gran velocidad (unos 20.000 km/s), la fuerzas eléctricas serían muy débiles e insuficientes para conseguir desviar las partículas alfa.
Además, para atravesar la lámina del metal, estas partículas se encontrarían con muchos átomos, que irían compensando las desviaciones hacia diferentes direcciones.
Pero se observó que un pequeño porcentaje de partículas se desviaban hacia la fuente de polonio, aproximadamente una de cada 8.000 partícula al utilizar una finísima lámina de oro con unos 200 átomos de espesor. En palabras de Rutherford ese resultado era "tan sorprendente como si le disparases balas de cañón a una hoja de papel y rebotasen hacia ti".
Rutherford concluyó que el hecho de que la mayoría de las partículas atravesaran la hoja metálica, indica que gran parte del átomo está vacío, que la desviación de las partículas alfa indica que el deflector y las partículas poseen carga positiva, pues la desviación siempre es dispersa. Y el rebote de las partículas alfa indica un encuentro directo con una zona fuertemente positiva del átomo y a la vez muy densa.
El modelo atómico de Rutherford mantenía el planteamiento de Thomson, de que los átomos poseen electrones, pero su explicación sostenía que todo átomo estaba formado por un núcleo y una corteza. El núcleo debía tener carga positiva, un radio muy pequeño y en él se concentraba casi toda la masa del átomo. La corteza estaría formada por una nube de electrones que orbitan alrededor del núcleo.
Según Rutherford, las órbitas de los electrones no estaban muy bien definidas y formaban una estructura compleja alrededor del núcleo, dándole un tamaño y forma indefinida. También calculó que el radio del átomo, según los resultados del experimento, era diez mil veces mayor que el núcleo mismo, lo que implicaba un gran espacio vacío en el átomo.

Este es un video con el modelo atomico de Rutherford
Un video mas explicandonos sobre el modelo de rutherford, los eespectros de onda en el hidrogeno, y algo del modelo de thomson
Como ya vimos, fue muy importante los descubrimientos que se hicieron anteriores al modelo de rutherford como la radaiactividad, el efecto fotoelectrico, el descubrimiento de los isotopos y los espectros de onda
Veamos un poco mas sobre estos temas para comprender como es que visualizaban al tomo en aquellos tiempos
Primero veamos el trabajo sobre la radiacion de Marie Curie
Marie Curie

Marie y Pierre estudiaron los materiales radiactivos, en particular el uranio en forma de pechblenda, que tenía la curiosa propiedad de ser más radiactiva que el uranio que se extraía de ella. La explicación lógica fue suponer que la pechblenda contenía trozos de algún elemento mucho más radiactivo que el uranio.
También descubren que el torio podía producir radioactividad. Tras varios años de trabajo constante, a través de la concentración de varias clases de pechblenda, aislaron dos nuevos elementos químicos. El primero, en 1898, fue nombrado como polonio en referencia a su país nativo. Polonia había sido particionado en el s. XVIII entre Rusia, Prusia y Austria, y la esperanza de Skłodowska-Curie fue nombrarlo al elemento con su país nativo para atraer la atención hacia su pérdida de independencia. El Polonio fue el primer elemento químico nombrado por razones políticas.,[3] y el otro, radio debido a su intensa radiactividad. Siempre trabajaron en estos años en un cobertizo y Pierre era el encargado de suministrar todos los medios y artilugios para que Marie trabajara. Pierre tenía temporadas de gran fatiga que incluso le obligaba a reposar en cama, además de que los dos sufren quemaduras y llagas producidas por sus peligrosos trabajos radiactivos.
Poco después Marie obtuvo un gramo de cloruro de radio, lo que consiguió al tener que manipular hasta ocho toneladas de pechblenda. En 1902 presentan el resultado y les invitan a todos los sitios, a todas las cenas y reuniones, lo que les lleva a la fama. Los científicos les mandaban cartas y los estadounidenses les pedían que dieran a conocer todos sus descubrimientos. Tanto Pierre como Marie aceptan y prestan todas sus investigaciones sin querer lucrarse de ello mediante patentes, un hecho que es aplaudido por todo el mundo.
Premios Nobel
Junto con Pierre Curie y Henri Becquerel, Marie fue galardonada con el Premio Nobel de Física en 1903, "en reconocimiento de los extraordinarios servicios rendidos en sus investigaciones conjuntas sobre los fenómenos de radiación descubierta por Henri Becquerel". Fue la primera mujer que obtuvo tal galardón. Les dieron 15.000 dólares, parte de los cuales lo utilizaron para hacer regalos a sus familias y en comprarse una bañera. Un tiempo después Pierre obtuvo una cátedra en la Sorbona. La fama les abrumó y se concentraron en sus trabajos. En 1904 tuvo su segunda hija, Eve, pero antes había tenido un aborto, probablemente producido por la radioactividad.
El 19 de abril de 1906 ocurrió una tragedia: Pierre fue atropellado por un carruaje de seis toneladas, murió sin que nada se pudiera hacer por él. Marie quedó muy afectada, pero quería seguir con sus trabajos y rechazó una pensión vitalicia. Además asumió la cátedra de su marido, y fue la primera mujer en dar clases en la universidad en los 650 años transcurridos desde su fundación.
En 1910 demostró que se podía obtener un gramo de radio puro. Al año siguiente recibió el Premio Nobel de Química «en reconocimiento de sus servicios en el avance de la Química por el descubrimiento de los elementos radio y polonio, el aislamiento del radio y el estudio de la naturaleza y compuestos de este elemento»,. Con una actitud desinteresada, no patentó el proceso de aislamiento del radio, dejándolo abierto a la investigación de toda la comunidad científica.
Marie Curie fue la primera persona a la que se le concedieron dos Premios Nobel en dos diferentes campos. La otra persona que lo ha obtenido hasta el presente es Linus Pauling (química y paz). Dos premios Nobel en el mismo campo lo han obtenido John Bardeen (física) y Frederick Sanger (química). Marie Curie presidió, por otra parte, el Instituto del Radio y trabajó en el gran laboratorio Curie.
Ahora vamos con Frederick Soddy y su descubrimiento sobre los isotopos
Frederick Soddy

Frederick Soddy (n. Eastbourne, Inglaterra, 2 de septiembre de 1877 - † Brighton, 22 de septiembre de 1956) fue un químico y profesor universitario inglés
Investigaciones científicas
Rutherford y él se dieron cuenta de que el comportamiento anómalo de elementos radioactivos era debido al hecho de que se transformaban en otros elementos y que producían radiaciones alfa, beta y gamma. En 1903, con Sir William Ramsay, Soddy verifícó que la desintegración del radio producía helio.
Desde 1904 a 1914, fue profesor en la Universidad de Glasgow y fue allí donde mostró que el uranio se transformaba en radio. Fue ahí también donde demostró que los elementos radioactivos pueden tener más de un peso atómico, a pesar de que sus propiedades químicas sean idénticas; esto le llevó al concepto de isótopo. Soddy demostró más tarde que también los elementos químicos no radioactivos pueden tener múltiples isótopos. Demostró además que un átomo puede moverse hacia abajo dos lugares en su peso atómico emitiendo rayos alfa y uno hacia arriba emitiendo rayos beta. Esto supuso un paso fundamental en el conocimiento de la relación entre las familias de elementos radioactivos.
Estas investigaciones permitieron el descubrimiento del elemento radiactivo llamado protactinio, que realizaron independientemente Soddy en Inglaterra y Otto Hann y Lise Meitner en Alemania.
En 1921 fue galardonado con el premio Nobel de Química por sus notables contribuciones al conocimiento de la química radiactiva y las investigaciones sobre la existencia y naturaleza de los isótopos.
los dejo con un video sobre que son los isotopos y algunas de sus aplicaciones
Seguimos con el efecto Fotoelectrico descubierto por Philipp Lenard
Philipp Lenard

Philipp Eduard Anton von Lenard, en húngaro Fülöp Lénárd, (n. Presburgo, actual Bratislava, 7 de junio de 1862 – Messelhausen, Baden-Württemberg, 20 de mayo de 1947) fue un físico alemán de origen austro-húngaro, ganador del premio Nobel de Física en 1905 por sus investigaciones sobre los rayos catódicos y el descubrimiento de muchas de sus propiedades
Investigaciones científicas [editar]Trabajó inicialmente en mecánica, publicando los Principios de Mecánica, junto con Hertz, en 1894. Posteriormente se interesó en la fosforescencia y la luminiscencia. También realizó estudios del magnetismo. También publicó artículos sobre la oscilación de las gotas de agua precipitadas.
En 1888, cuando trabajaba en Heidelberg junto con Quincke, realizó sus primeros trabajos con los rayos catódicos, tratando de descubrir si era cierto que, como suponía Hertz, eran análogos a la luz ultravioleta y podrían, al igual que éstos, pasar a través de una ventana de cuarzo en la pared de un tubo de descarga. Descubrió que no ocurría así, pero más adelante, en 1892, cuando trabajaba como ayudante de Hertz en Bonn, descubrió que era posible separar, por medio de una placa fina de aluminio, dos espacios, uno en el que los rayos catódicos se producían y otro en el que se podían observar. Es lo que se conoce como “ventana de Lenard”, consistente en sustituir la placa de cuarzo que hasta entonces se utilizaba para cerrar el tubo de descarga por una fina placa de aluminio capaz de mantener el vacío dentro del tubo y permitir que los rayos catódicos pasasen hacia fuera. De esta forma era posible estudiar los rayos catódicos, y también la fluorescencia que causaban fuera del tubo de descarga. Aunque Lenard inicialmente, siguiendo las ideas de Hertz, suponía que los rayos catódicos se propagaban en el éter, más tarde abandonó este punto de vista como resultado de los trabajos de Perrin, J.J. Thomson y Wien, quienes demostraron la naturaleza corpuscular de los rayos catódicos.
Más tarde, Lenard amplió los trabajos de Hertz sobre el efecto fotoeléctrico, demostrando que cuando la luz ultravioleta incide en el vacío sobre ciertos metales arranca electrones del metal. Estos electrones se propagan en el vacío, pudiendo ser acelerados o retardados por un campo eléctrico, y sus trayectorias se pueden curvar por un campo magnético. Mediante medidas exactas demostró que el número de electrones arrancados (intensidad de corriente eléctrica) es proporcional a la intensidad (o número de fotones) de la luz del incidente, mientras que la velocidad de los electrones, es decir, su energía cinética, es independiente del número de electrones y depende únicamente de la longitud de onda (y por tanto, de la frecuencia y energía) de la radiación incidente.
Estos hechos estaban en contradicción con los postulados de la física clásica y no pudieron ser explicados hasta 1905, cuando Einstein elaboró su teoría del efecto fotoeléctrico basada en el concepto del cuanto de luz (fotón).
El 1905 fue galardonado con el Premio Nobel de Física por sus trabajos alrededor de los rayos catódicos.
Algunos de los premios y reconocimientos que recibió fueron, además del Premio Nobel de Física en 1905:
La medalla Franklin, en 1905.
Doctor honoris causa por la Universidad de Christiania (Oslo) en 1911.
Doctor honoris causa por la Universidad de Dresde en 1922.
El protector del águila del Reich alemán en 1933.
Doctor honoris causa por la Universidad de Presburgo en 1942.
Este es un video sobre el efecto Fotoelectrico en el se hace mencion a Einstein que tambien investigo sobre el efecto fotoelctrico, al cual le dio una mejor explicacion qeu la de Lenard
Les dejo otro video del Efecto fotoelctrico
Vamos con Max Planck y el decubrimiento sobre la relacion de entre la cantidad de energia y de frecuencia asociada a una particula
Max Planck

Max Karl Ernest Ludwig Planck (Kiel, Alemania, 23 de abril de 1858 – Gotinga, Alemania, 4 de octubre de 1947) fue un físico alemán considerado como el fundador de la teoría cuántica y galardonado con el Premio Nobel de Física en 1918.
Investigaciones científicas
Aunque en un principio fue ignorado por la comunidad científica, profundizó en el estudio de la teoría del calor y descubrió, uno tras otro, los mismos principios que ya había enunciado Josiah Willard Gibbs (sin conocerlos previamente, pues no habían sido divulgados). Las ideas de Clausius sobre la entropía ocuparon un espacio central en sus pensamientos.
En 1900, descubrió una constante fundamental, la denominada Constante de Planck, usada para calcular la energía de un fotón. Planck establece que la energía se radia en unidades pequeñas denominadas cuantos. La ley de Planck relaciona que la energía de cada cuanto es igual a la frecuencia de la radiación multiplicada por la Constante de Planck. Un año después descubrió la ley de radiación del calor, denominada Ley de Planck, que explica el espectro de emisión de un cuerpo negro. Esta ley se convirtió en una de las bases de la teoría cuántica, que emergió unos años más tarde con la colaboración de Albert Einstein y Niels Bohr.
En 1905 se publicaron los primeros estudios del desconocido Albert Einstein acerca de la teoría de la relatividad, siendo Planck unos de los pocos científicos que reconocieron inmediatamente lo significativo de esta nueva teoría científica.
Planck también contribuyó considerablemente a ampliar esta teoría. La hipótesis de Einstein sobre la ligereza del quantum (el fotón), basada en el descubrimiento de Philipp Lenard de 1902 sobre el efecto fotoeléctrico, fue rechazada inicialmente por Planck, así como la teoría de James Clerk Maxwell sobre electrodinámica.
En 1910 Einstein precisó el comportamiento anómalo del calor específico en bajas temperaturas como otro ejemplo de un fenómeno que desafía la explicación de la física clásica. Planck y Walther Nernst para clarificar las contradicciones que aparecían en la física organizó la primera Conferencia Solvay, realizada en Bruselas en 1911. En esta reunión, Einstein finalmente convenció a Planck sobre sus investigaciones y sus dudas. A partir de aquel momento les unió una gran amistad, siendo nombrado Albert Einstein profesor de física en la universidad de Berlín mientras que Planck fue decano.
En 1918 fue galardonado con el Premio Nobel de Física «por su papel jugado en el avance de la física con el descubrimiento de la teoría cuántica».
Constante de Planck
La constante de Planck, simbolizada con la letra h (o bien ħ=h/2π, en cuyo caso se conoce como constante reducida de Planck), es una constante física que representa al cuanto elemental de acción. Es la relación entre la cantidad de energía y de frecuencia asociadas a un cuanto o a una partícula. Desempeña un papel central en la teoría de la mecánica cuántica y recibe su nombre de su descubridor, Max Planck, uno de los padres de dicha teoría.
Les dejo un video sobre la velocidad de la luz que tambien tiene relacion con los espectros de onda,la enrgis de las particulas y la constante de planck
Vamos con el espectro de lus visible y los estudios de Gustav Kirchhoff y sobre la espectroscopia
Gustav Kirchhoff

Gustav Robert Kirchhoff (12 de marzo de 1824 - 17 de octubre de 1887) fue un físico prusiano cuyas principales contribuciones científicas estuvieron en el campo de los circuitos eléctricos, la teoría de placas, la óptica, la espectroscopia y la emisión de radiación de cuerpo negro. Kirchhoff propuso el nombre de radiación de cuerpo negro en 1862. Es responsable de dos conjuntos de leyes fundamentales en la teoría clásica de circuitos eléctricos y en la emisión térmica. Aunque ambas se denominan Leyes de Kirchhoff, probablemente esta denominación es más común en el caso de las Leyes de Kirchhoff de la ingeniería eléctrica.
Las tres leyes de la espectroscopia de Kirchhoff
Más adelante propuso las tres leyes empíricas que describen la emisión de luz por objetos incandescentes:
Un objeto sólido caliente produce luz en espectro continuo.
Un gas tenue produce luz con líneas espectrales en longitudes de onda discretas que dependen de la composición química del gas.
Un objeto sólido a alta temperatura rodeado de un gas tenue a temperaturas inferiores produce luz en un espectro continuo con huecos en longitudes de onda discretas cuyas posiciones dependen de la composición química del gas.
La justificación de estas leyes fue dada más tarde por Niels Bohr, contribuyendo decisivamente al nacimiento de la mecánica cuántica.
Espectro visible
Se denomina espectro visible a la región del espectro electromagnético que el ojo humano es capaz de percibir. A la radiación electromagnética en este rango de longitudes de onda se le llama luz visible o simplemente luz. No hay límites exactos en el espectro visible; un típico ojo humano responderá a longitudes de onda desde 400 a 700 nm aunque algunas personas pueden ser capaces de percibir longitudes de onda desde 380 a 780 nm.
Espectroscopia
Los estudios científicos de objetos basados en el espectro de luz que emiten es llamado espectroscopia. Una aplicación particularmente importante de éste estudio es en la astronomía donde los espectroscopios son esenciales para analizar propiedades de objetos distantes. La espectroscopía astronómica utiliza difracción de alta dispersión para observar espectros a muy altas resoluciones espectrales. El helio fue lo primero que se detectó en el análisis del espectro del sol; los elementos químicos pueden ser detectados en objetos astronómicos por las líneas espectrales y las líneas de absorción; la medida de líneas espectrales puede ser usada como medidas de corrimiento al rojo o corrimiento al azul de objetos distantes que se mueven a altas velocidades. El primer exoplaneta en ser descubierto fue el encontrado por el análisis de efecto Doppler de estrellas a las que su alta resolución que variaba su velocidad radial tan pequeñas como unos pocos metros por segundo podrían ser detectadas: la presencia de planetas fue revelada por su influencia gravitacional en las estrellas analizadas
El espectro visible por los humanos
Artículo principal: Espectro visible
El espectro electromagnético está constituido por todos los posibles niveles de energía de la luz. Hablar de energía es equivalente a hablar de longitud de onda; por ello, el espectro electromagnético abarca todas las longitudes de onda que la luz puede tener. De todo el espectro, la porción que el ser humano es capaz de percibir es muy pequeña en comparación con todas las existentes. Esta región, denominada espectro visible, comprende longitudes de onda desde los 380 nm hasta los 780 nm ( 1nm = 1 nanómetro = 0,000001 mm). La luz de cada una de estas longitudes de onda es percibida en el cerebro humano como un color diferente. Por eso, en la descomposición de la luz blanca en todas sus longitudes de onda, mediante un prisma o por la lluvia en el arco iris, el cerebro percibe todos los colores.

Por tanto, del Espectro visible, que es la parte del espectro electromagnético de la luz solar que podemos notar, cada longitud de onda es percibida en el cerebro como un color diferente.
Newton uso por primera vez la palabra espectro (del latín, "apariencia" o "aparición") en 1671 al describir sus experimentos en óptica. Newton observó que cuando un estrecho haz de luz solar incide sobre un prisma de vidrio triangular con un ángulo, una parte se refleja y otra pasa a través del vidrio y se desintegra en diferentes bandas de colores. También Newton hizo converger esos mismos rayos de color en una segunda lente para formar nuevamente luz blanca. Demostró que la luz solar tiene todos los colores del arco iris.
Cuando llueve y luce el sol, cada gota de lluvia se comporta igual que el prisma de Newton y de la unión de millones de gotas de agua se forma el fenómeno del arco iris.
A pesar que el espectro es continuo y por lo tanto no hay cantidades vacías entre uno y otro color, se puede establecer la siguiente aproximación
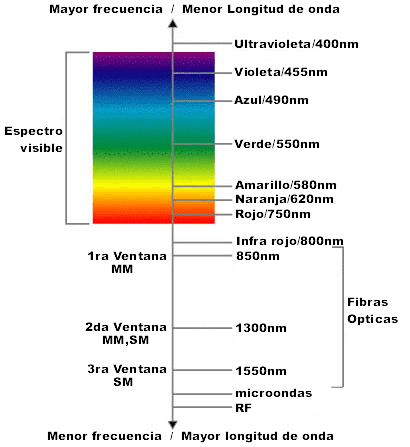
Espectro de absorción
El espectro de absorción de un material muestra la fracción de la radiación electromagnética incidente que un material absorbe dentro de un rango de frecuencias. Es, en cierto sentido, el opuesto de un espectro de emisión. Cada elemento químico posee líneas de absorción en algunas longitudes de onda, hecho que está asociado a las diferencias de energía de sus distintos orbitales atómicos. De hecho, se emplea el espectro de absorción para identificar los elementos componentes de algunas muestras, como líquidos y gases; más allá, se puede emplear para determinar la estructura de compuestos orgánicos. Un ejemplo de las implicaciones de un espectro de absorción es que aquél objeto que lo haga con los colores azul, verde y amarillo aparecerá de color rojo cuando incida sobre él luz blanca.
Espectro de emisión
El espectro de emisión de un elemento son las radiaciones emitidas por éste, en estado gaseoso, cuando se le comunica energía. Si colocamos un tubo con hidrógeno calentado a alta temperatura, esto produce que emita radiaciones, y cuando éstas se hacen pasar a través de un prisma de cuarzo se refractan, y se desvían. Cuando salen del prisma, las radiaciones se encuentran separadas en la placa detectora.
Espectro atómico
El espectro de emisión atómica de un elemento es un conjunto de frecuencias de las ondas electromagnéticas emitidas por átomos de ese elemento. Cada espectro de emisión atómico de un átomo es único y puede ser usado para determinar si ese elemento es parte de un compuesto desconocido.
Las características del espectro de emisión de algunos elementos son claramente visibles a ojo descubierto cuando estos elementos son calentados. Por ejemplo, cuando un alambre de platino es bañado en una solución de nitrato de estroncio y después es introducido en una llama, los átomos de estroncio emiten color rojo. De manera similar, cuando el cobre es introducido en una llama, ésta se convierte en luz azul. Estas caracterizaciones determinadas permiten identificar los elementos mediante su espectro de emisión atómica.
El hecho de que sólo algunos colores aparezcan en las emisiones atómicas de los elementos significa que sólo determinadas frecuencias de luz son emitidas. Cada una de estas frecuencias están relacionadas con la energía con la fórmula:
E=hf
donde E es la energía, h es la constante de Planck y v es la frecuencia. La frecuencia v es igual a: v=c/λ. Donde c es la velocidad de la luz en el vacio y λ es la longitud de onda. Con esto se concluye que sólo algunos fotones con ciertas energías son emitidos por el átomo. El principio del espectro de emisión atómica explica la variedad de colores en signos de neón, así como los resultados de las pruebas de las llamas químicas mencionadas anteriormente.
Las frecuencias de luz que un átomo puede emitir depende de los estados en que los electrones pueden estar. Cuando están excitados, los electrones se mueven hacia una capa de energía superior. Y cuando caen hacia su capa normal emiten la luz.
Veamos lo que es un espectrometro
Espectrómetro
El Espectrómetro es un aparato capaz de analizar el espectro característico de un movimiento ondulatorio. Se aplica a variados instrumentos que operan sobre un amplio campo de longitudes de onda.
Un espectrómetro óptico o espectroscopio, es un instrumento que sirve para medir las propiedades de la luz en una determinada porción del espectro electromagnético. La variable que se mide generalmente es la intensidad de la luz pero se puede medir también el estado de polarización, por ejemplo. La variable independiente suele ser la longitud de onda de la luz, generalmente expresada en submúltiplos del metro, aunque alguna vez pueda ser expresada en cualquier unidad directamente proporcional a la energía del fotón, como la frecuencia o los electrón-voltios, que mantienen un relación inversa con la longitud de onda. Se utilizan espectrómetros en espectroscopia para producir líneas espectrales y medir sus longitudes de onda e intensidades.
En general, un instrumento concreto sólo operará sobre una pequeña porción de éste campo total, debido a las diferentes técnicas necesarias para medir distintas porciones del espectro. Por debajo de las frecuencias ópticas (es decir, microondas, radio y audio), el analizador de espectro es un dispositivo electrónico muy parecido.
les dejo con un video sobre los espectros de luz
Un video sobre el espectro elctromagnetico
Muchos de estos descubrimientos sirvieron de base para la creacion del modelo atomico de Bhor. Ahora nos enfocaremos en el modelo atomico de Bhor posterior al modelo de Rutherford, como un ultimo dato (lo considero importante) les dejare sobre el primer hombre que hizo una transmutacion artifial (Reaccion nuclear artificial)
o sea, Rutherford
En 1914 empieza la Primera Guerra Mundial, y Rutherford se concentra en los métodos acústicos de detección de submarinos. Tras la guerra, ya en 1919, lleva a cabo su primera transmutación artificial. Después de observar los protones producidos por el bombardeo de hidrógeno de partículas alfa (al observar el parpadeo que producen en pantallas cubiertas de sulfuro de zinc), se da cuenta de que obtiene muchos de esos parpadeos si realiza el mismo experimento con aire y aún más con nitrógeno puro. Deduce de ello que las partículas alfa, al golpear los átomos de nitrógeno, han producido un protón, es decir que el núcleo de nitrógeno ha cambiado de naturaleza y se ha transformado en oxígeno, al absorber la partícula alfa. Rutherford acababa de producir la primera transmutación artificial de la historia. Algunos opinan que fue el primer alquimista que consiguió su objetivo
Bueno sin mas que agregar pasemos al modelo atomico de Bhor
Modelo atómico de Bohr
El modelo atómico de Bohr o de Bohr-Rutherford es un modelo cuantizado del átomo que Bohr propuso en 1913 para explicar cómo los electrones pueden tener órbitas estables alrededor del núcleo. Este modelo planetario es un modelo funcional que no representa el átomo (objeto físico) en sí sino que explica su funcionamiento por medio de ecuaciones.
Niels Bohr se basó en el átomo de hidrógeno para realizar el modelo que lleva su nombre. Bohr intentaba realizar un modelo atómico capaz de explicar la estabilidad de la materia y los espectros de emisión y absorción discretos que se observan en los gases. Describió el átomo de hidrógeno con un protón en el núcleo, y girando a su alrededor un electrón. El modelo atómico de Bohr partía conceptualmente del modelo atómico de Rutherford y de las incipientes ideas sobre cuantización que habían surgido unos años antes con las investigaciones de Max Planck y Albert Einstein. Debido a su simplicidad el modelo de Bohr es todavía utilizado frecuentemente como una simplificación de la estructura de la materia.
En este modelo los electrones giran en órbitas circulares alrededor del núcleo, ocupando la órbita de menor energía posible, o la órbita más cercana posible al núcleo. El electromagnetismo clásico predecía que una partícula cargada moviéndose de forma circular emitiría energía por lo que los electrones deberían colapsar sobre el núcleo en breves instantes de tiempo. Para superar este problema Bohr supuso que los electrones solamente se podían mover en órbitas específicas, cada una de las cuales caracterizada por su nivel energético. Cada órbita puede entonces identificarse mediante un número entero n que toma valores desde 1 en adelante. Este número "n" recibe el nombre de Número Cuántico Principal.
Bohr supuso además que el momento angular de cada electrón estaba cuantizado y sólo podía variar en fracciones enteras de la constante de Planck. De acuerdo al número cuántico principal calculó las distancias a las cuales se hallaba del núcleo cada una de las órbitas permitidas en el átomo de hidrógeno.
Estos niveles en un principio estaban clasificados por letras que empezaban en la "K" y terminaban en la "Q". Posteriormente los niveles electrónicos se ordenaron por números. Cada órbita tiene electrones con distintos niveles de energía obtenida que después se tiene que liberar y por esa razón el electrón va saltando de una órbita a otra hasta llegar a una que tenga el espacio y nivel adecuado, dependiendo de la energía que posea, para liberarse sin problema y de nuevo volver a su órbita de origen.
Sin embargo no explicaba el espectro de estructura fina que podría ser explicado algunos años más tarde gracias al modelo atómico de Sommerfeld. Históricamente el desarrollo del modelo atómico de Bohr junto con la dualidad onda-corpúsculo permitiría a Erwin Schrödinger descubrir la ecuación fundamental de la mecánica cuántica.
Postulados de Bohr
En 1913, Niels Bohr desarrolló su célebre modelo atómico de acuerdo a cuatro postulados fundamentales:
Los electrones orbitan el átomo en niveles discretos y cuantizados de energía, es decir, no todas las órbitas están permitidas, tan sólo un número finito de éstas.
Los electrones pueden saltar de un nivel electrónico a otro sin pasar por estados intermedios.
El salto de un electrón de un nivel cuántico a otro implica la emisión o absorción de un único cuanto de luz (fotón) cuya energía corresponde a la diferencia de energía entre ambas órbitas.
Las órbitas permitidas tienen valores discretos o cuantizados
La cuarta hipótesis asume que el valor mínimo de n es 1. Este valor corresponde a un mínimo radio de la órbita del electrón de 0.0529 nm. A esta distancia se le denomina radio de Bohr. Un electrón en este nivel fundamental no puede descender a niveles inferiores emitiendo energía.
Se puede demostrar que este conjunto de hipótesis corresponde a la hipótesis de que los electrones estables orbitando un átomo están descritos por funciones de onda estacionarias. Un modelo atómico es una representación que describe las partes que tiene un átomo y como están dispuestas para formar un todo.
Basándose en la constante de Planck consiguió cuantizar las órbitas observando las líneas del espectro.
modelo atomico de Bhor

Les dejo unos videos sobre el modelo atomico de Bhor
les dejo un video sobre lo que hemos visto hasta ahora de modelos atomicos
Despues de que Bhor publicara su modelo atomico, siguieron descubrimientos importantes sobre el atomo, veamos algunos de estos.
Francis Aston confirmo el descubrimiento de los isotopos de Soddy
Francis Aston

Francis William Aston (n. Birmingham, 1 de septiembre de 1877 - † Londres, 20 de noviembre de 1945) fue un físico, químico y profesor universitario inglés.
En 1903 obtuvo una beca para estudiar en la Universidad de Birmingham. En 1909 se trasladó al Laboratorio Cavendish en Cambridge, invitado por Joseph John Thomson, donde trabajó en la identificación de los isótopos del neón e investigó las descargas eléctricas en tubos de baja presión. Posteriormente fue profesor en el Trinity College de Cambridge y en 1921 ingresó en la Royal Society y en 1935 fue elegido presidente del Comité Atómico Internacional.
Volvió a estos estudios tras la I Guerra Mundial en 1919, e inventó un espectrógrafo de masas que le permitió descubrir, a causa de las diferencias de masa, un cierto número de isótopos en elementos no radiactivos, que le permitieron identificar no menos de 212 de los 287 isótopos naturales.
En 1922 fue galardonado con el premio Nobel de Química por el descubrimiento de un gran número de isótopos no radioactivos mediante un espectógrafo de masas.
Entre sus obras se encuentran Isotopes (1922) y Mass-Spectra and Isotopes (1933).
Espectrómetro de masas
La espectrometría de masas es una técnica experimental que permite la medición de iones derivados de moléculas. El espectrómetro de masas es un instrumento que permite analizar con gran precisión la composición de diferentes elementos químicos e isótopos atómicos, separando los núcleos atómicos en función de su relación masa-carga (m/z). Puede utilizarse para identificar los diferentes elementos químicos que forman un compuesto, o para determinar el contenido isotópico de diferentes elementos en un mismo compuesto. Con frecuencia se encuentra como detector de un cromatógrafo de gases, en una técnica híbrida conocida por sus iniciales en inglés, GC-MS.
El espectrómetro de masas mide razones carga/masa de iones, calentando un haz de material del compuesto a analizar hasta vaporizarlo e ionizar los diferentes átomos. El haz de iones produce un patrón específico en el detector, que permite analizar el compuesto. En la industria es altamente utilizado en el análisis elemental de semiconductores, biosensores y cadenas poliméricas complejas.
Espectrometro de masas

ahora vamos con Henri Mosley
Henry Moseley

Henry Gwyn Jeffreys Moseley (23 de noviembre, 1887 – 10 de agosto, 1915) fue un químico y físico inglés. Su principal contribución a la ciencia, fue la justificación cuantitativa del concepto de número atómico en la Ley de Moseley, en química avanzada proporcionó un apoyo fundamental al modelo de Bohr definido con detalle por Rutherford/Antonius Van den Broek mencionando que los núcleos atómicos contienen cargas positivas iguales a su número atómico.
Moseley nació en Weymouth, en la costa sur de Inglaterra en el año 1887. Su padre fue un naturalista, un profesor de Anatomía en Oxford y miembro de la Challenger Expedition. Atendió a las clases del Eton College durante su edad escolar. En 1906 entró en el Trinity College, Oxford|Trinity College de la Universidad de Oxford, y para la graduación desde el instituto en 1910 fue a la Manchester University para trabajar con Ernest Rutherford. Durante este primer año en Manchester, tuvo una carga lectiva completa, pero tras este año empezó tener cada vez más tiempo para dedicar a la investigación.
En el año 1914 se retiró de Manchester para volver a Oxford con el objetivo de continuar en su carrera de investigación, pero la Primera Guerra Mundial cambió sus intenciones y se alistó en la división de Royal Engineers. Fue destinado a Gallípoli (lugar donde se celebró la Batalla de Gallípoli) y fue asesinado por un francotirador en el año en 1915 (la causa fue un disparo en la cabeza cuando estaba telegrafiando una orden). Muchos historiadores especulan que debería haber ganado un Premio Nobel, pero esto es imposible ya que el premio sólo se concede a los investigadores vivos. Se ha especulado que a causa de la muerte de Moseley es la razón por la que el gobierno inglés durante la segunda guerra mundial y en la actualidad prohíbe el alistamiento de científicos en el ejército en época de guerra.
Moseley murió cuando tenía sólo veintisiete años, Moseley, en opinión de muchos científicos, pudo haber contribuido al conocimiento de más detalles de la estructura de la materia si hubiera vivido más tiempo. Como dijo una vez Niels Bohr en el año 1962, Puedes ver hoy en día que el trabajo de Rutherford sobre el núcleo atómico no hubiera sido tomado en serio. Tampoco lo hubiéramos entendido hoy en día si no hubiéramos tenido las investigaciones de Moseley
Ley de Moseley
La Ley de Moseley es una ley empírica que establece una relación sistemática entre la longitud de onda de los rayos X emitidos por distintos átomos con su número atómico. Fue enunciada en 1913 por el físico británico Henry Moseley.
Tuvo una gran importancia histórica, pues hasta ese momento, el número atómico era sólo el lugar que ocupaba un elemento en la tabla periódica. Dicho lugar había sido asociado a cada elemento de modo semi-arbitario por Mendeleiev y no estaba relacionado cuantitativamente hasta entonces con ninguna cantidad física medible.
Moseley considera la energía que debe poseer un fotón al ser emitido en una transición de nivel energético mayor a uno menor. La energía la calcula a partir del modelo atómico de Bohr y tomando en cuenta el apantallamiento sufrido por el electrón (que va realizar la transición) debido a la carga nuclear.
Despues de estos importantes descubrimientos sigamos entonces con el modeloa tomico de Sommerfield el cual fue publicado solo unos pocos años despues que el modelo de Bhor
Modelo atómico de Sommerfield
El modelo atómico de Sommerfeld es un modelo atómico hecho por el físico alemán Arnold Sommerfeld (1868-1951) que básicamente es una generalización relativista del modelo atómico de Bohr (1913).
El modelo atómico de Bohr funcionaba muy bien para el átomo de hidrógeno. Sin embargo, en los espectros realizados para átomos de otros elementos se observaba que electrones de un mismo nivel energético tenían distinta energía, mostrando que algo andaba mal en el modelo. Su conclusión fue que dentro de un mismo nivel energético existían subniveles, es decir, energías ligeramente diferentes para un nivel energético dado.
Además desde el punto de vista teórico, Sommerfeld había encontrado que en ciertos átomos las velocidades de los electrones alcanzaban una fracción apreciable de la velocidad de la luz. Sommerfeld estudió la cuestión para electrones relativistas.
En 1916, Sommerfeld perfeccionó el modelo atómico de Bohr intentando paliar los dos principales defectos de éste. Para eso introdujo dos modificaciones básicas: Órbitas cuasi-elípticas para los electrones y velocidades relativistas. En el modelo de Bohr los electrones sólo giraban en órbitas circulares. La excentricidad de la órbita dio lugar a un nuevo número cuántico: el número cuántico azimutal, que determina la forma de los orbitales, se lo representa con la letra l y toma valores que van desde 0 hasta n-1. Las órbitas con:
l = 0 se denominarían posteriormente orbitales s o sharp
l = 1 se denominarían 2 p o principal.
l = 2 se denominarían d o diffuse.
l = 3 se denominarían f o fundamental.
Para hacer coincidir las frecuencias calculadas con las experimentales, Sommerfeld postuló que el núcleo del átomo no permanece inmóvil, sino que tanto el núcleo como el electrón se mueven alrededor del centro de masas del sistema, que estará situado muy próximo al núcleo al tener este una masa varios miles de veces superior a la masa del electrón.
Para explicar el desdoblamiento de las líneas espectrales, observando al emplear espectroscopios de mejor calidad, Sommerfeld supone que las orbitas del electrón pueden ser circulares y elípticas. Introduce el número cuántico secundario o azimutal, en la actualidad llamado l, que tiene los valores 0, 1, 2,…(n-1), e indica el momento angular del electrón en la orbita, determinando los subniveles de energía en cada nivel cuántico y la excentricidad de la orbita.
En 1916, Arnold Sommerfeld, con la ayuda de la relatividad de Albert Einstein, hizo las siguientes modificaciones al modelo de Bohr:
Los electrones se mueven alrededor del nucleo en orbitas circulares o elípticas.
A partir del segundo nivel energético existen dos o más subniveles en el mismo nivel.
El electrón es una corriente eléctrica minúscula.
En consecuencia el modelo atómico de Sommerfeld es una generalización del modelo atómico de Bohr desde el punto de vista relativista, aunque no pudo demostrar las formas de emisión de las órbitas elípticas, solo descartó su forma circular.
Despues de esto Vsmos con Louis-Victor de Broglie, el cual gracias a sus investigaciones constituyeron la base de el modelo atomico de Schrödinger
Louis-Victor de Broglie

Prince Louis-Victor Pierre Raymond de Broglie (n. Dieppe, Francia, 15 de agosto de 1892 - † París, Francia, 19 de marzo de 1987). Físico francés conocido a veces en castellano como Luis de Broglie.
La naturaleza de la luz no es fácilmente analizable a no ser que la consideremos de tipo ondulatorio a fin de explicar ciertos fenómenos (como reflexión, refracción, difracción, etc.) o de tipo corpuscular al pretender hacerlo con otros (como el efecto fotoeléctrico, etc), ¿es posible que las partículas tengan también propiedades de onda?.
En 1924 Louis De Broglie extendio el carácter dual de la luz a los electrones, protones, neutrones, átomos y moléculas, y en general a todas las partículas materiales. Basandose en consideraciones relativostas y en la teoría cuántica pensó que si la luz se comportaba como onda y como partícula la materia debería poseer este carácter dual.
El movimiento de una partícula puede considerarse como el movimiento de un paquete de ondas, algo así como la superposición de varias ondas de longuitudes de onda poco diferentes, cuyas oscilaciones se intensifican al máximo en el punto del espacio ocupado popr la partícula. No hay nada de imaginario en estas ondas de materia, son tan reales como las ondas luminosas y las del sonido, aunque no sean observables en todos los casos, copmo ocurre con las ondas electromagnéticas, los aspectos ondulatorios y de partículas de los cuerpos en movimiento nunca se pueden observar al mismo tiempo.
les dejo un video con la relacion onda particula
Despues de esto seguimos con el modelo Atomico de Schrödinger
Modelo atómico de Schrödinger
El modelo atómico de Schrödinger es un modelo cuántico no relativista. Se basa en la solución de la ecuación de Schrödinger para un potencial electrostático con simetría esférica, llamado también átomo hidrogenoide.
El modelo de Bohr funcionaba muy bien para el átomo de hidrógeno. En los espectros realizados para otros átomos se observaba que electrones de un mismo nivel energético tenían energías ligeramente diferentes. Esto no tenía explicación en el modelo de Bohr, y sugería que se necesitaba alguna corrección. La propuesta fue que dentro de un mismo nivel energético existían subniveles. La forma concreta en que surgieron de manera natural estos subniveles, fue incorporando órbitas elípticas y correcciones relativistas. Así, en 1916, Arnold Sommerfeld modificó el modelo atómico de Bohr, en el cual los electrones sólo giraban en órbitas circulares, al decir que también podían girar en órbitas elípticas más complejas y calculó los efectos relativistas.
El modelo atómico de Schrödinger concebía originalmente los electrones como ondas de materia. Así la ecuación se interpretaba como la ecuación ondulatoria que describía la evolución en el tiempo y el espacio de dicha onda material. Más tarde Max Born propuso una interpretación probabilística de la función de onda de los electrones. Esa nueva interpretación es compatible con los electrones concebidos como partículas cuasipuntuales cuya probabilidad de presencia en una determinada región viene dada por la integral del cuadrado de la función de onda en una región.
El modelo atómico de Schrödinger predice adecuadamente las líneas de emisión espectrales, tanto de átomos neutros como de átomos ionizados.igualmente predice adecuadamente la modificación de los niveles energéticos cuando existe un campo magnético o eléctrico (efecto Zeeman y efecto Stark respectivamente). Además, con ciertas modificaciones semiheurísticas el modelo explica el enlace químico y la estabilidad de las moléculas. Cuando se necesita una alta precisión en los niveles energéticos puede emplearse un modelo similar al de Schrödinger, pero donde el electrón es descrito mediante la ecuación relativista de Dirac en lugar de mediante la ecuación de Schrödinger.
Sin embargo, el nombre de "modelo atómico" de Schrödinger puede llevar a confusión ya que no explica la estructura completa del átomo. El modelo de Schrödinger explica sólo la estructura electrónica del átomo y su interacción con la estructura electrónica de otros átomos, pero no explica como es el núcleo atómico ni su estabilidad.
Les dejo un video sobre los numeros cuanticos
Vamos con Heisenberg y el principio de incertidumbre
En mecánica cuántica, la relación de indeterminación de Heisenberg o principio de incertidumbre afirma que no se puede determinar, simultáneamente y con precisión arbitraria, ciertos pares de variables físicas, como son, por ejemplo, la posición y el momento lineal (cantidad de movimiento) de un objeto dado. En otras palabras, cuanta mayor certeza se busca en determinar la posición de una partícula, menos se conoce su cantidad de movimiento lineal y, por eso depende, su velocidad. Esto implica que las partículas, en su movimiento, no tienen asociada una trayectoria bien definida. Este principio fue enunciado por Werner Heisenberg en 1927.
les dejo un video sobre el principio de incertidumbre
Por ultimo vamos con James Chadwick que descubrio el neutron en 1932
James Chadwick
Sir James Chadwick (20 de octubre de 1891 – 24 de julio de 1974) fue un físico inglés laureado con el Premio Nobel.
En 1932, Chadwick realizó un descubrimiento fundamental en el campo de la ciencia nuclear: descubrió la partícula en el núcleo del átomo que pasaría a llamarse neutrón, esta partícula no tiene carga eléctrica. En contraste con el núcleo de helio (partículas alfa) que está cargado positivamente y por lo tanto son repelidas por las fuerzas eléctricas del núcleo de los átomos pesados, esta nueva herramienta para la desintegración atómica no necesitaba sobrepasar ninguna barrera electrónica, y es capaz de penetrar y dividir el núcleo de los elementos más pesados. De esta forma, Chadwick allanó el camino hacia la fisión del uranio 235 y hacia la creación de la bomba atómica. Como premio por su descubrimiento se le otorgó la Medalla Hughes de la Royal Society en 1932 y el Premio Nobel de física en 1935. También descubrió el tritio.
Más tarde descubrió que un científico alemán había identificado al neutrón al mismo tiempo. Sin embargo, Hans Falkenhagen temía publicar sus resultados. Cuando Chadwick supo del descubrimimento de Falkenhagen le ofreció compartir el Premio Nobel. Falkenhagen, sin embargo, lo rechazó. James Chadwick murio el 24 de julio de 1974.
les dejo unos videos con los descubrimientos que dieron paso a la identificacion de las particulas elemntales del atomo
Aqui les dejo unos videos sobre todo lo que hemos visto del atomo y sus modelos
No hay comentarios:
Publicar un comentario